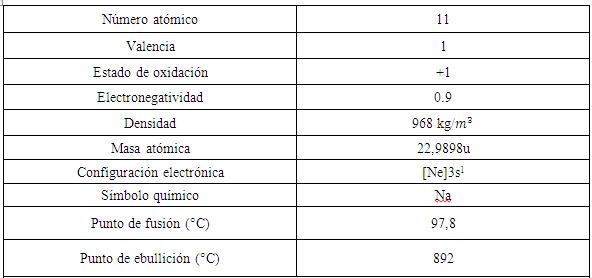
Sodio
El sodio es uno de los metales alcalinos más comunes en la tierra, es muy común en los siguientes compuestos; sal marina, sal roca, carbonatos y nitratos. Este metal ocupa el sexto lugar en su abundancia en la corteza terrestre. La palabra sodio tiene diferentes orígenes como "neter" en la Bliblia, la palabra "natrón" en latín, la palabra "refresco "en Egipto. Por otra parte en la edad media se le denominó soda, la palabra natrium proviene del alemán y en la actualidad se lo reconoce como Na (MOREAU, S.F.).
El sodio tiene una textura suave, su color es blanco, brillante y plateado en su estado de oxidación. Es un metal muy reactivo, se oxida con la presencia del oxígeno y tiende a tener una reacción impulsiva con el agua. También se puede decir que la mayoría de los minerales están compuestos por el sodio y este es un componente esencial para la vida humana.
Tabla 4: estructura atómica del sodio.
Batería de ión sodio
Las baterías de ion sodio son dispositivos de almacenamiento de energía de un tipo de batería reusable que utiliza iones de sodio como portadores de carga. Las sales de grado de sodio son mucho más abundantes que el de litio en la naturaleza y son mucho más baratos. También estas baterías serán más amigables con el medio ambiente, y más fácil de reciclar. Por sus características tienden a convertirse en una alternativa rentable, especialmente para aplicaciones como en almacenamiento de energía en red para fuentes de energías renovables como la energía eólica y solar (Khun, 2014).
Para el funcionamiento de una batería ión-sodio fig x, "se utiliza un ánodo de conversión óxido de hierro recubierto con carbono, un cátodo de intercalación en láminas de sodio, y un electrólito de perclorato de sodio (NaClO4) en una solución de carbonato de fluoroetileno y metanosulfonato de etilo (CH3SO3C2H5)" (Ibáñez, 2014). Su funcionamiento es igual al de iones de litio ya que durante la descarga, los iones de sodio se transportan desde el ánodo al cátodo, mientras que los electrones pasan al cátodo a través de un circuito externo.
Tabla 5 sistemas de batería de sodio.

En el sistema de baterías de sodio tanto la batería de sodio-cloruro de níquel como la de sodio-azufre están compuestas por un electrolito sólido de cerámica de aluminio conductor de iones. Para poder intervenir en una reacción química los electrolitos solidos se deben disolver o fundir en temperatura bastante alta. La temperatura de servicio para los dos sistemas es de 300oC aunque la batería de sodio-cloruro puede seguir funcionando a temperaturas aún más bajas que las de sodio-azufre. Con los sistemas de batería de sodio tabla 2 puede desarrollarse vehículos eléctricos superior a 100km (Reverte, 1999).
"El rendimiento del prototipo presentado hoy con 90 vatios-hora / kilogramo, su densidad de energía (la cantidad de electricidad que puede ser almacenada por kilogramo de la batería) es comparable a ciertas baterías de iones de litio, tales como la batería de Li-ion de hierro / fosfato, y que su vida (número máximo de ciclos de carga y descarga) es superior a 2000 ciclos" (Cailloce, 2015).
La compañía estadounidense Aquion Energy, ha desarrollado baterías de ion-sodio con capacidades bastantes reconocibles de 5000 ciclos de carga y descarga, usando un ánodo de carbón, magnesio con sodio para en cátodo y agua como electrolito ya que este puede ayudar en el transporte de iones de sodio entre los electrodos mientras ocurre la carga y la descarga (Velasco, 2011).
En cuanto al ciclo de vida de esta batería se puede decir que es muy similar al de litio. Las perspectivas comerciales para estas baterías son bastantes convenientes, por lo cual se espera que el mercado mundial el 2020 pueda llegar $80 mil millones, el doble de hoy. Muchas compañías utilizan baterías de tipo plomo ácido por su bajo coste, pero su tiene capacidad de descarga es muy bajo en comparación al de sodio y las baterías de litio tienen un costo bastante numeroso, por lo tanto esta sería una opción para abrir camino a nuevas tecnologías como son las de la batería de sodio informa (Cailloce, 2015).